Obsah
Co jsou onkogeny?
Onkogen je buněčný gen, jehož exprese pravděpodobně podporuje rozvoj rakoviny. Jaké jsou různé typy onkogenů? Jakými mechanismy se aktivují? Vysvětlení.
Co je onkogen?
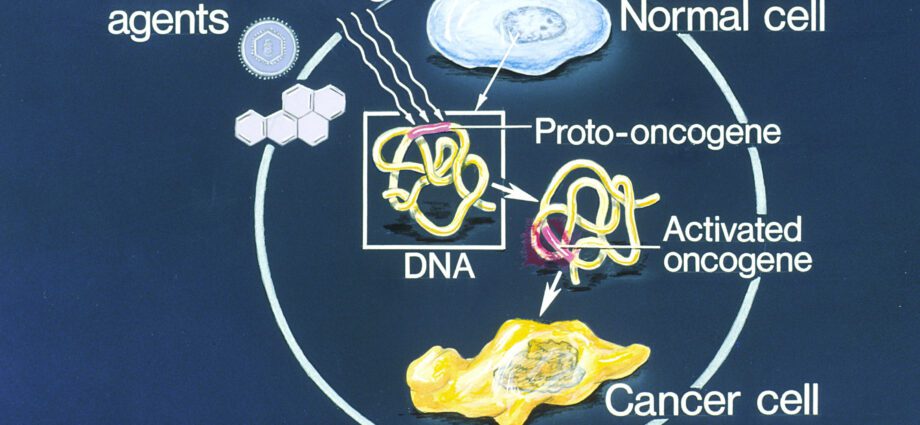
Onkogen (z řeckého onkos, tumor a genos, narození) také nazývaný protoonkogen (c-onc) je gen, jehož exprese pravděpodobně uděluje rakovinný fenotyp normální eukaryotické buňce. Onkogeny skutečně řídí syntézu proteinů, které stimulují buněčné dělení (nazývané onkoproteiny) nebo inhibují programovanou buněčnou smrt (nebo apoptózu). Onkogeny jsou zodpovědné za nekontrolovanou buněčnou proliferaci predisponující k rozvoji rakovinných buněk.
Onkogeny jsou rozděleny do 6 tříd, které odpovídají onkoproteinům, které kódují:
- růstové faktory. Příklad: protoonkogen kódující proteiny rodiny FGF (Fibroblast Growth Factor);
- receptory transmembránového růstového faktoru. Příklad: protoonkogen erb B, který kóduje receptor EGF (epidermální růstový faktor);
- G-proteiny nebo membránové proteiny vázající GTP. Příklad: protoonkogeny rodiny ras;
- membránové tyrosin proteinové kinázy;
- proteinové kinázy membrány;
- proteiny s jadernou aktivitou.Příklad: protoonkogeny erb A, phos, červen et c-myc.
Jaká je role onkogenů?
Buněčnou obnovu zajišťuje buněčný cyklus. Ten je definován sadou událostí, které generují dvě dceřiné buňky z mateřské buňky. Mluvíme o buněčné dělení nebo „mitóza“.
Buněčný cyklus musí být regulován. Pokud není buněčné dělení dostatečné, organismus nefunguje optimálně; Naopak, pokud je buněčné dělení hojné, buňky se nekontrolovaně množí, což podporuje vzhled rakovinných buněk.
Regulace buněčného cyklu je zaručena geny zařazenými do dvou kategorií:
- anti-onkogeny, které inhibují buněčnou proliferaci zpomalením buněčného cyklu;
- protoonkogeny (c-onc) nebo onkogeny, které podporují buněčnou proliferaci aktivací buněčného cyklu.
Pokud porovnáme buněčný cyklus s autem, anti-onkogeny by byly brzdy a protoonkogeny by byly jejich urychlovači.
Anomálie, patologie spojené s onkogeny
Vzhled nádor může být důsledkem mutace inaktivující anti-onkogeny nebo naopak z mutace aktivující protoonkogeny (nebo onkogeny).
Ztráta funkce anti-onkogenů jim brání v provádění jejich inhibiční aktivity buněčné proliferace. Inhibice anti-onkogenů je otevřenými dveřmi nekontrolovaného dělení buněk, což může vést ke vzniku maligních buněk.
Anti-onkogeny jsou však buněčné geny, to znamená, že jsou přítomny duplicitně na dvojici chromozomů, které je nesou v jádře buňky. Když tedy jedna kopie anti-onkogenu není funkční, druhá umožňuje působit jako brzda, takže subjekt je chráněn proti buněčné proliferaci a proti riziku nádorů. To je například případ genu BRCA1, jehož inhibiční mutace odhaluje rakovinu prsu. Pokud je však druhá kopie tohoto genu funkční, pacient zůstává chráněn, i když je náchylný kvůli vadné první kopii. Jako součást takové predispozice je někdy zvažována preventivní dvojitá mastektomie.
Naopak aktivační mutace ovlivňující protoonkogeny zvýrazňuje jejich stimulační účinek na buněčnou proliferaci. Tato anarchická buněčná proliferace predisponuje k rozvoji rakoviny.
Stejně jako anti-onkogeny jsou pro-onkogeny buněčné geny přítomné ve dvojicích na dvojici chromozomů, které je nesou. Na rozdíl od anti-oncongenů je však přítomnost jediného mutovaného pro-onkogenu dostatečná k vyvolání obávaných účinků (v tomto případě buněčné proliferace). Pacient nesoucí tuto mutaci je tedy ohrožen rakovinou.
Mutace v onkogenech mohou být spontánní, dědičné nebo dokonce způsobené mutageny (chemikálie, UV paprsky atd.).
Aktivace onkogenů: zahrnuté mechanismy
Na počátku aktivačních mutací onkogenů nebo proonkogenů (c-onc) je několik mechanismů:
- virová integrace: inzerce viru DNA na úrovni regulačního genu. To je například případ lidského papilomaviru (HPV), který je sexuálně přenosný;
- bodová mutace v sekvenci genu kódujícího protein;
- delece: ztráta většího nebo menšího fragmentu DNA, která je příčinou genetické mutace;
- strukturální přestavba: chromozomální alterace (translokace, inverze) vedoucí k tvorbě hybridního genu kódujícího nefunkční protein;
- amplifikace: abnormální násobení počtu kopií genu v buňce. Tato amplifikace obecně vede ke zvýšení úrovně exprese genu;
- deregulace exprese RNA: geny jsou odpojeny od svého normálního molekulárního prostředí a umístěny pod nevhodnou kontrolu jiných sekvencí způsobujících modifikaci jejich exprese.
Příklady onkogenů
Geny kódující růstové faktory nebo jejich receptory:
- PDGF: kóduje růstový faktor krevních destiček spojený s gliomem (rakovina mozku);Erb-B: kóduje receptor epidermálního růstového faktoru. Souvisí s glioblastomem (rakovina mozku) a rakovinou prsu;
- Erb-B2 také nazývaný HER-2 nebo neu: kóduje receptor růstového faktoru. Souvisí s rakovinou prsu, slinných žláz a vaječníků;
- RET: kóduje receptor růstového faktoru. Souvisí s rakovinou štítné žlázy.
Geny kódující cytoplazmatická relé ve stimulačních cestách:
- Ki-ras: spojený s rakovinou plic, vaječníků, tlustého střeva a slinivky;
- N-ras: spojený s leukémií.
Geny kódující transkripční faktory, které aktivují růst podporující geny:
- C-myc: spojený s leukémií a rakovinou prsu, žaludku a plic;
- N-myc: spojený s neuroblastomem (rakovina nervových buněk) a glioblastomem;
- L-myc: spojený s rakovinou plic.
Geny kódující jiné molekuly:
- Hcl-2: kóduje protein, který normálně blokuje sebevraždu buněk. Spojeno s lymfomy B lymfocytů;
- Bel-1: také pojmenovaný PRAD1. Kóduje Cyclin DXNUMX, aktivátor hodin buněčného cyklu. Souvisí s rakovinou prsu, hlavy a krku;
- MDM2: kóduje antagonistu proteinu produkovaného tumor supresorovým genem.
- P53: spojený se sarkomy (rakoviny pojivové tkáně) a dalšími druhy rakoviny.
Zaměřte se na viry ocongene
Onkogenní viry jsou viry, které mají schopnost přeměnit buňku, kterou infikují, na rakovinu. 15% rakovin má virovou etiologii a tyto virové rakoviny jsou příčinou přibližně 1.5 milionu nových případů ročně a 900 úmrtí ročně na celém světě.
Přidružené virové rakoviny jsou problémem veřejného zdraví:
- papilomavirus je spojen s téměř 90% rakovin děložního čípku;
- 75% všech hepatocarcinomů je spojeno s virem hepatitidy B a C.
Existuje pět kategorií onkogenních virů, ať už jde o RNA viry nebo DNA viry.
RNA viry
- Retroviridae (HTVL-1) vás vystavuje riziku T leukémie;
- Flaviviridae (virus hepatitidy C) je ohrožen hepatocelulárním karcinomem.
DNA viry
- Papovaviridae (papilomavirus 16 a 18) vystavuje rakovině děložního čípku;
- Herpesviridae (virus Esptein Barr) vystavuje B lymfomu a karcinomu;
- Herpesviridae (lidský herpesvirus 8) je vystaven Kaposiho chorobě a lymfomům;
- Hepadnaviridae (virus hepatitidy B) je citlivý na hepatocelulární karcinom.